Cổ phiếu MRNA giảm trong phiên sau giờ khi FDA chính thức “phanh” một chương trình mà giới đầu tư xem là một trong những “cầu nối sản phẩm” khả dĩ nhất của Moderna ngoài mảng COVID.
Trung tâm Đánh giá và Nghiên cứu Sinh phẩm (CBER) của cơ quan này đã gửi thư Từ chối thụ lý hồ sơ (Refusal-to-File - RTF) đối với Đơn xin cấp giấy phép sinh phẩm (BLA) của Moderna cho vắc-xin cúm mùa đang nghiên cứu, mRNA-1010. CBER cũng cho biết sẽ không khởi động quy trình xem xét.

Dù vậy, Moderna cho biết thư này không nêu bất kỳ vấn đề nào về an toàn hay hiệu quả của bản thân vắc-xin, và điểm vướng nằm ở nhóm so sánh được sử dụng trong nghiên cứu hiệu quả Giai đoạn 3.
Khi tiến độ ra mắt một sản phẩm chủ chốt trở nên kém rõ ràng, thị trường thường định giá lại rủi ro rất nhanh – phản ánh tâm lý thận trọng tương tự như đợt cổ phiếu Atlassian ($TEAM) về mức giá 2018 dù doanh thu tăng – đặc biệt trong phiên sau giờ khi thanh khoản mỏng hơn.
Chuyện gì đã xảy ra với cổ phiếu MRNA sau giờ giao dịch?
| Mục |
Mức / Chi tiết |
| Đóng cửa phiên chính |
~$42.00 |
| Giá sau giờ giao dịch (ví dụ) |
~$38.27 (-8.88%) |
| Biên độ trong ngày |
~$41.68 đến ~$45.50 |
| Biên độ 52 tuần |
~$22.28 đến ~$55.20 |
Cổ phiếu MRNA đóng cửa quanh mức $42.00, rồi giảm về khoảng $38.27 trong giao dịch sau giờ, tương đương mức giảm khoảng 8.9% tại thời điểm ghi nhận.
Nguyên nhân chính là gì?

FDA từ chối tiếp nhận hồ sơ đơn xin vắc-xin cúm của Moderna
Moderna cho biết họ đã nhận được thư từ Trung tâm Đánh giá và Nghiên cứu Sinh phẩm (CBER) thuộc FDA, trong đó nêu rõ CBER sẽ không khởi động việc xem xét Đơn xin cấp giấy phép sinh phẩm (BLA) cho mRNA-1010 và thay vào đó sẽ ban hành thư Từ chối thụ lý hồ sơ (RTF).
Công ty nhấn mạnh rằng họ đã sử dụng Phiếu Xét duyệt Ưu tiên (Priority Review Voucher) để đảm bảo tiến độ xem xét đúng hạn. Việc bị từ chối lần này đặc biệt khiến thị trường thất vọng, vì nó cho thấy vấn đề không chỉ đơn giản là “đang xếp hàng chờ”.
Moderna cũng nói thêm rằng quyết định từ chối này đi ngược với phản hồi mà công ty nhận được trong các buổi tham vấn trước Giai đoạn 3 và trước khi nộp hồ sơ. Vì vậy, Moderna đã đề nghị một cuộc họp Type A để làm rõ hướng đi tiếp theo.
Thư Từ chối thụ lý hồ sơ là gì?
RTF là một công cụ chính thức mà FDA dùng để tránh lãng phí thời gian thẩm định đối với những bộ hồ sơ mà cơ quan cho rằng chưa đầy đủ hoặc chưa phù hợp để tiến hành một đánh giá có ý nghĩa ngay tại thời điểm nộp hồ sơ.
Theo quy trình nội bộ của FDA, RTF là cách để ngăn việc xem xét không cần thiết đối với các hồ sơ chưa hoàn chỉnh. Hành động RTF giúp bên nộp hồ sơ khắc phục những “thiếu sót nghiêm trọng” trước khi nộp lại một bộ hồ sơ hoàn chỉnh, từ đó hồ sơ mới có thể được xem xét chuyên sâu.
Có hai điểm thực tế quan trọng đối với nhà giao dịch:
RTF không đồng nghĩa với phê duyệt, và cũng không phải là một quyết định từ chối sau khi đã hoàn tất thẩm định toàn diện.
Con đường phía trước sẽ phụ thuộc vào các thay đổi mà FDA yêu cầu và tốc độ phản hồi của công ty.
Tại sao FDA nói không với vắc-xin cúm của Moderna?

Vấn đề cốt lõi, theo nhiều bản tin, là FDA không coi thiết kế nghiên cứu của Moderna là “đầy đủ và được kiểm soát tốt” vì nhóm so sánh không phản ánh cách FDA nhìn nhận về tiêu chuẩn chăm sóc tốt nhất hiện có, đặc biệt đối với người cao tuổi.
Theo các bản tin, Moderna đã so sánh mRNA-1010 với một vắc-xin cúm đã được cấp phép dạng liều tiêu chuẩn (thường được nhắc tới là Fluarix của GSK trong các bài viết).
Trong khi đó, FDA ám chỉ họ kỳ vọng một nhóm so sánh phù hợp hơn với thực hành tiêm chủng phổ biến tại Hoa Kỳ đối với nhóm nguy cơ cao, đặc biệt là người từ 65 tuổi trở lên (thường là các phiên bản tăng cường hoặc liều cao).
Moderna không đồng tình với động thái này. Trong tuyên bố của mình, công ty cho biết thư RTF không nêu lo ngại về an toàn hay hiệu quả và mô tả quyết định này là không nhất quán với các phản hồi trước đó từ FDA.
Các lập luận chính của Moderna (trích từ thông cáo của công ty)
FDA viện dẫn việc dùng chất đối chứng liều tiêu chuẩn là lý do duy nhất để từ chối khởi động quá trình xem xét.
Moderna cho biết FDA không đưa ra các lo ngại cụ thể về an toàn hoặc hiệu quả.
Moderna đã đề nghị một cuộc họp Loại A với lãnh đạo FDA để làm rõ lộ trình tiếp theo.
Moderna cho biết công ty không kỳ vọng quyết định này sẽ ảnh hưởng tới kế hoạch đầu tư dài hạn hay dự báo tài chính năm 2026 của họ.
Tại sao vấn đề đối chứng lại quan trọng?
Trong các thử nghiệm vắc-xin, chất đối chứng là sản phẩm “chuẩn nền” dùng để đối chiếu khi đánh giá hiệu suất của sản phẩm mới. Nếu cơ quan quản lý cho rằng đối chứng không đại diện cho tiêu chuẩn phù hợp trong thực tế, họ có thể lập luận rằng bằng chứng hiện có chưa trả lời đúng câu hỏi mà họ cần được giải đáp.
Đây là lý do thị trường phản ứng mạnh, ngay cả khi công ty nói rằng không có lo ngại an toàn mới. Trọng tâm tranh luận dịch chuyển từ “Vắc-xin có hiệu quả không?” sang “Bằng chứng hiện tại có đáp ứng tiêu chuẩn của FDA cho nhóm dân số này ở thời điểm này hay không?”
Điều đó cũng lý giải vì sao giới giao dịch thường coi tiêu đề RTF là một “sự kiện về tiến độ”. Vắc-xin vẫn có thể ra thị trường, nhưng mốc thời gian trở nên khó dự đoán hơn.
Điều này có ý nghĩa gì đối với lộ trình vắc-xin cúm của Moderna
Moderna cho biết mRNA-1010 hiện đang được xem xét tại EU, Canada và Australia. Công ty dự báo các phê duyệt sớm nhất ở những khu vực này có thể diễn ra vào cuối 2026 hoặc đầu 2027, dựa trên tiến độ đánh giá hiện tại.
Tại Hoa Kỳ, bước đi tiếp theo sẽ phụ thuộc vào kết quả của cuộc họp Loại A. Cuộc họp này sẽ quyết định liệu Moderna có cần nộp lại Đơn xin cấp phép thuốc sinh học (BLA) kèm dữ liệu bổ sung, đổi cách tiếp cận, hoặc điều chỉnh cách trình bày để đáp ứng kỳ vọng của FDA về chất đối chứng hay không.
Tại sao phản ứng cổ phiếu MRNA lại diễn ra nhanh như vậy: Nó mở lại một mối lo ngại quen thuộc của Moderna
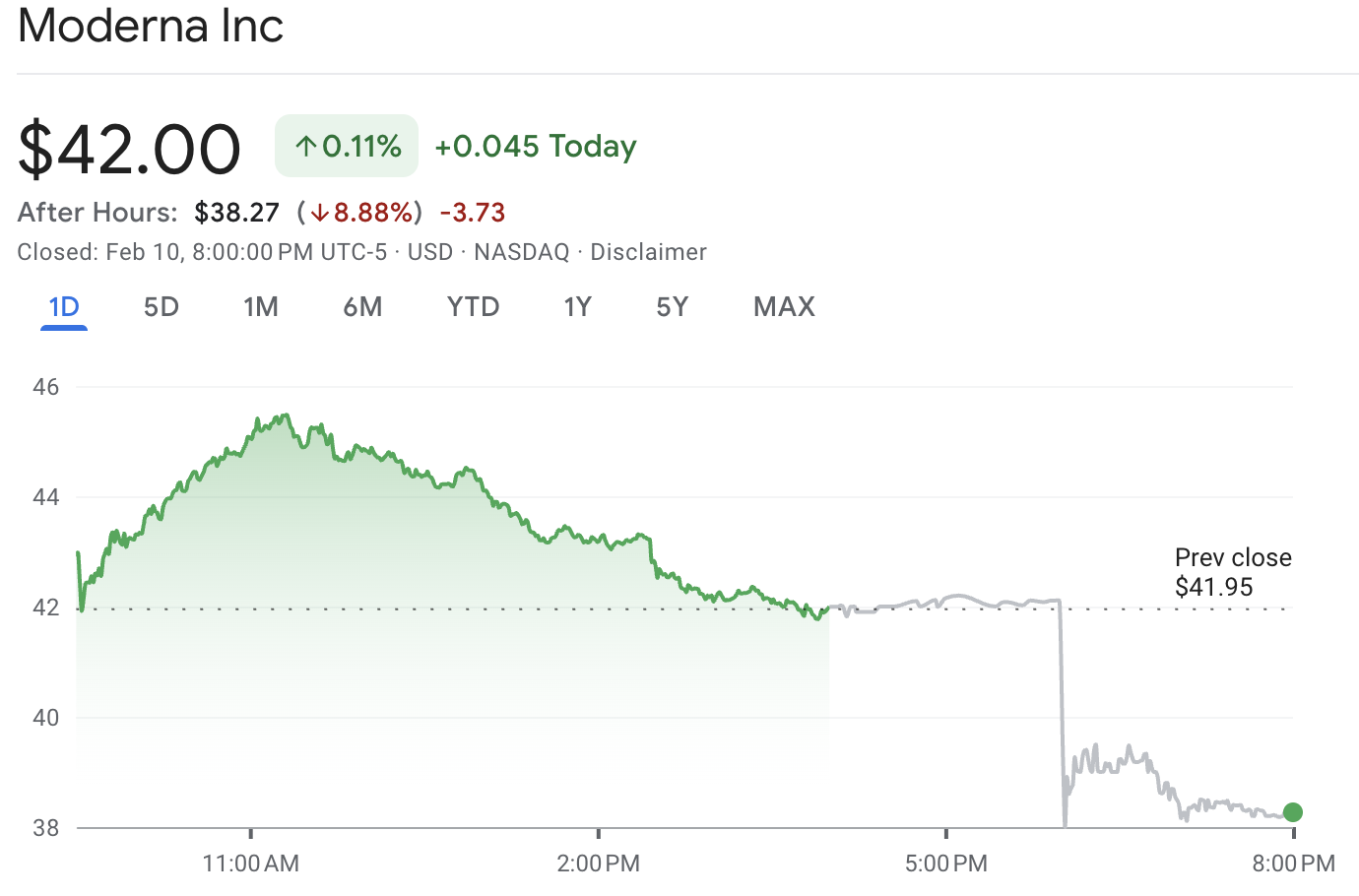
MRNA đã nỗ lực thuyết phục nhà đầu tư rằng tương lai hậu COVID của công ty được xây dựng trên một danh mục sản phẩm, thay vì phụ thuộc vào một sản phẩm đơn lẻ. Cúm giữ vai trò trung tâm trong câu chuyện đó vì đây là thị trường bệnh hô hấp theo mùa lớn, lặp lại hằng năm và đã được chứng minh về mặt thương mại.
Quyết định từ chối của FDA lần này buộc câu chuyện đó phải “thiết lập lại” trên ba phương diện.
1) Nó đẩy lùi một lộ trình ra mắt ngắn hạn tại Hoa Kỳ
Ngay cả khi vấn đề có thể xử lý được, một RTF đồng nghĩa Moderna hiện không có quy trình xem xét nào đang chạy tại FDA. Chỉ riêng điều đó đã làm giảm khả năng nhìn thấy trong ngắn hạn và nới rộng khoảng cách giữa “dữ liệu” và “doanh thu”.
2) Nó tăng độ không chắc chắn xung quanh chiến lược kết hợp về bệnh hô hấp của Moderna
Moderna từng rút hồ sơ nộp FDA cho vắc-xin kết hợp cúm và COVID mRNA-1083 sau khi FDA yêu cầu thêm dữ liệu về hiệu quả chống cúm trước khi tiến hành xem xét. Chi tiết này quan trọng vì thị trường đã chứng kiến lộ trình hô hấp của Moderna từng “trượt nhịp” một lần.
3) Nó báo hiệu một tiêu chuẩn khắt khe hơn cho các chất đối chứng vắc-xin hô hấp
Nếu FDA hiện nhấn mạnh rằng chất đối chứng phải là “tiêu chuẩn chăm sóc tốt nhất có sẵn” cho người lớn tuổi, thì đây không còn là chuyện của riêng một chương trình. Điều này có thể định hình cách các công ty thiết kế thử nghiệm cúm trong tương lai và tốc độ họ có thể cải tiến sản phẩm.
Tại sao tiêu đề này có thể lan sang phản ứng đối với báo cáo thu nhập tiếp theo
Ngày công bố kết quả kinh doanh tiếp theo của MRNA được lên lịch vào ngày 13 tháng 2 năm 2026. Tương tự như sự chú ý dành cho Coca-Cola công bố KQKD và 5 yếu tố biến động giá vừa qua, định giá quyền chọn của MRNA đang phản ánh mức biến động ẩn hàng tuần dự kiến khoảng 11.63% trước cửa sổ sự kiện đó.
Biến động ẩn vượt 10% thường cho thấy nhà đầu tư đang dự liệu mức độ bất định đáng kể. Điều này gợi nhớ đến diễn biến vì sao giá cổ phiếu APP tăng vọt trước báo cáo lợi nhuận, khi các yếu tố tâm lý và vị thế thị trường tác động mạnh trước giờ G.
Sau một sự kiện FDA từ chối thụ lý hồ sơ, thị trường thường có xu hướng làm hai việc:
Đòi hỏi ngôn ngữ rõ ràng hơn về lộ trình tiến tới và các mốc thời gian.
Định giá lại biến động ẩn nếu thị trường kỳ vọng thông tin tiếp theo, chẳng hạn kết quả cuộc họp FDA, sẽ xuất hiện trong cùng khung thời gian.
Phân tích kỹ thuật cổ phiếu MRNA: Các mức mà nhà giao dịch nên theo dõi tối nay
| Chỉ báo |
Giá trị |
Tín hiệu |
| RSI (14) |
48.155 |
Trung tính |
| MACD (12,26) |
0.29 |
Mua |
| ATR (14) |
0.9374 |
Độ biến động cao |
| ADX (14) |
40.829 |
Bán |
Xét trên góc độ phân tích biểu đồ kỹ thuật, MRNA trên khung ngày nhìn chung vẫn ở trạng thái trung tính, khi các chỉ báo và đường trung bình động đang cho tín hiệu trái chiều tại thời điểm giá biến động trong phiên sau giờ.
Các mốc Pivot (Cổ điển)
| Loại mức |
Mức giá |
Cách nhà giao dịch thường sử dụng nó sau một tiêu đề |
| S1 (Cổ điển) |
$41.74 |
Vùng đầu tiên nơi lực mua bắt đáy có thể thử “ra tay” nếu thị trường ổn định lại. |
| S2 (Cổ điển) |
$41.31 |
Nếu thủng xuống dưới, khả năng cao giá sẽ quay lại kiểm tra các vùng hỗ trợ sâu hơn. |
| S3 (Cổ điển) |
$40.51 |
Một “đường” then chốt vì nằm gần vùng hội tụ của các đường trung bình động dài hạn. |
| Pivot (Cổ điển) |
$42.54 |
Việc quay trở lại phía trên pivot thường cho thấy thị trường đang bỏ qua trạng thái hoảng loạn ban đầu. |
| R1 (Cổ điển) |
$42.97 |
Mốc kiểm tra tăng đầu tiên nếu cổ phiếu hồi phục sau báo cáo lợi nhuận. |
| R2 (Cổ điển) |
$43.77 |
Một vùng hồi mạnh hơn, thường cần thêm sự “gỡ rối” về mặt cơ bản. |
Cách đọc thiết lập này:
Nếu cổ phiếu giữ được trên vùng thấp-$40 trong phiên thường, điều đó cho thấy bên mua vẫn đang bảo vệ xu hướng.
Nếu đà yếu trong phiên sau giờ lan sang phiên kế tiếp và giá vẫn nằm dưới các đường trung bình động chủ chốt, tâm lý thị trường có thể tiếp tục mong manh cho đến khi xuất hiện thông tin mới.
Các Câu hỏi Thường gặp (FAQ)
Tại sao cổ phiếu MRNA giảm sau giờ giao dịch hôm nay?
Trong phiên sau giờ, cổ phiếu MRNA giảm sau khi Moderna thông báo FDA đã gửi thư từ chối thụ lý hồ sơ (refusal-to-file) đối với đơn đăng ký BLA cho vắc-xin cúm mRNA-1010, đồng nghĩa FDA sẽ không khởi động quá trình xem xét.
FDA có cho rằng vắc-xin cúm của Moderna không an toàn không?
Không. Theo tuyên bố của Moderna, thư từ chối thụ lý hồ sơ không nêu ra bất kỳ mối lo ngại an toàn cụ thể nào liên quan đến mRNA-1010.
Tại sao FDA tập trung vào vắc-xin đối chứng?
Vì vắc-xin đối chứng là chuẩn so sánh để đánh giá hiệu suất, và FDA cho biết đối chứng được sử dụng không phản ánh “tiêu chuẩn chăm sóc tốt nhất hiện có,” đặc biệt với nhóm người cao tuổi.
Moderna có cho rằng điều này sẽ thay đổi dự báo năm 2026 của họ không?
Moderna cho biết họ không kỳ vọng quyết định từ chối thụ lý hồ sơ sẽ tác động đến dự báo tài chính năm 2026. Dù vậy, nhà đầu tư vẫn bán ra vì mốc thời gian tại Hoa Kỳ của chương trình cúm có ý nghĩa lớn đối với khả năng nhìn thấy doanh thu dài hạn.
Moderna còn có thể được chấp thuận ngoài Hoa Kỳ không?
Có. Moderna cho biết vắc-xin đã được chấp nhận để xem xét tại EU, Canada và Úc, với khả năng được phê duyệt dự kiến bắt đầu từ cuối 2026 hoặc đầu 2027.
Kết luận
Tóm lại, cổ phiếu MRNA giảm trong phiên sau giờ vì FDA đã gửi thư từ chối thụ lý hồ sơ đối với đơn đăng ký vắc-xin cúm mRNA của Moderna, qua đó làm gia tăng mức độ bất định ngắn hạn liên quan đến lộ trình tại Hoa Kỳ.
Điểm mấu chốt là động thái này liên quan đến quy trình phê duyệt và tiêu chuẩn thiết kế thử nghiệm, chứ không phải việc xuất hiện một rủi ro an toàn mới.
Yếu tố quyết định tiếp theo không nằm ở tranh luận về miễn dịch học cúm. Điều quan trọng tiếp theo là liệu Moderna có thể đạt được một lộ trình rõ ràng thông qua cuộc họp Type A với FDA hay không, và liệu lộ trình đó có đòi hỏi phải thực hiện thêm các thử nghiệm lâm sàng hay không. Cho đến khi có sự rõ ràng này, cổ phiếu MRNA nhiều khả năng vẫn sẽ là mục tiêu của phong cách giao dịch theo tin tức, biến động cao cho tới cửa sổ báo cáo thu nhập tiếp theo.
Tuyên bố miễn trừ trách nhiệm: Tài liệu này chỉ nhằm mục đích cung cấp thông tin chung và không nhằm là (và không nên được coi là) tư vấn tài chính, đầu tư hoặc các lời khuyên khác để dựa vào. Không có ý kiến nào trong tài liệu này cấu thành khuyến nghị của EBC hoặc tác giả rằng bất kỳ khoản đầu tư, chứng khoán, giao dịch hoặc chiến lược đầu tư cụ thể nào phù hợp với bất kỳ cá nhân nào.