Mulai Trading
Tentang EBC
Diterbitkan pada: 2026-03-18
Saham MRNA turun di perdagangan after-hours karena FDA memberikan penghentian tegas pada program yang oleh investor dianggap sebagai salah satu jembatan "produk berikutnya" Moderna yang paling realistis di luar waralaba COVID-nya.
Pusat Evaluasi dan Penelitian Biologis FDA (CBER) mengeluarkan surat Refusal-to-File (RTF) untuk biologics license application (BLA) Moderna untuk vaksin influenza musiman yang sedang diuji, mRNA-1010. Mereka juga mengatakan tidak akan memulai tinjauan.

Meskipun begitu, Moderna mengatakan surat itu tidak menimbulkan kekhawatiran tentang keamanan atau kemanjuran vaksin itu sendiri, dan bahwa masalahnya terkait dengan pembanding uji yang digunakan dalam studi efikasi Fase 3-nya.
Bagi para trader, itu sudah cukup untuk membuat saham bergerak cepat. Ketika garis waktu produk kunci menjadi kurang jelas, pasar cenderung menilai ulang risiko dengan cepat, terutama di perdagangan after-hours ketika likuiditas lebih tipis.
| Item | Tingkat / Rincian |
|---|---|
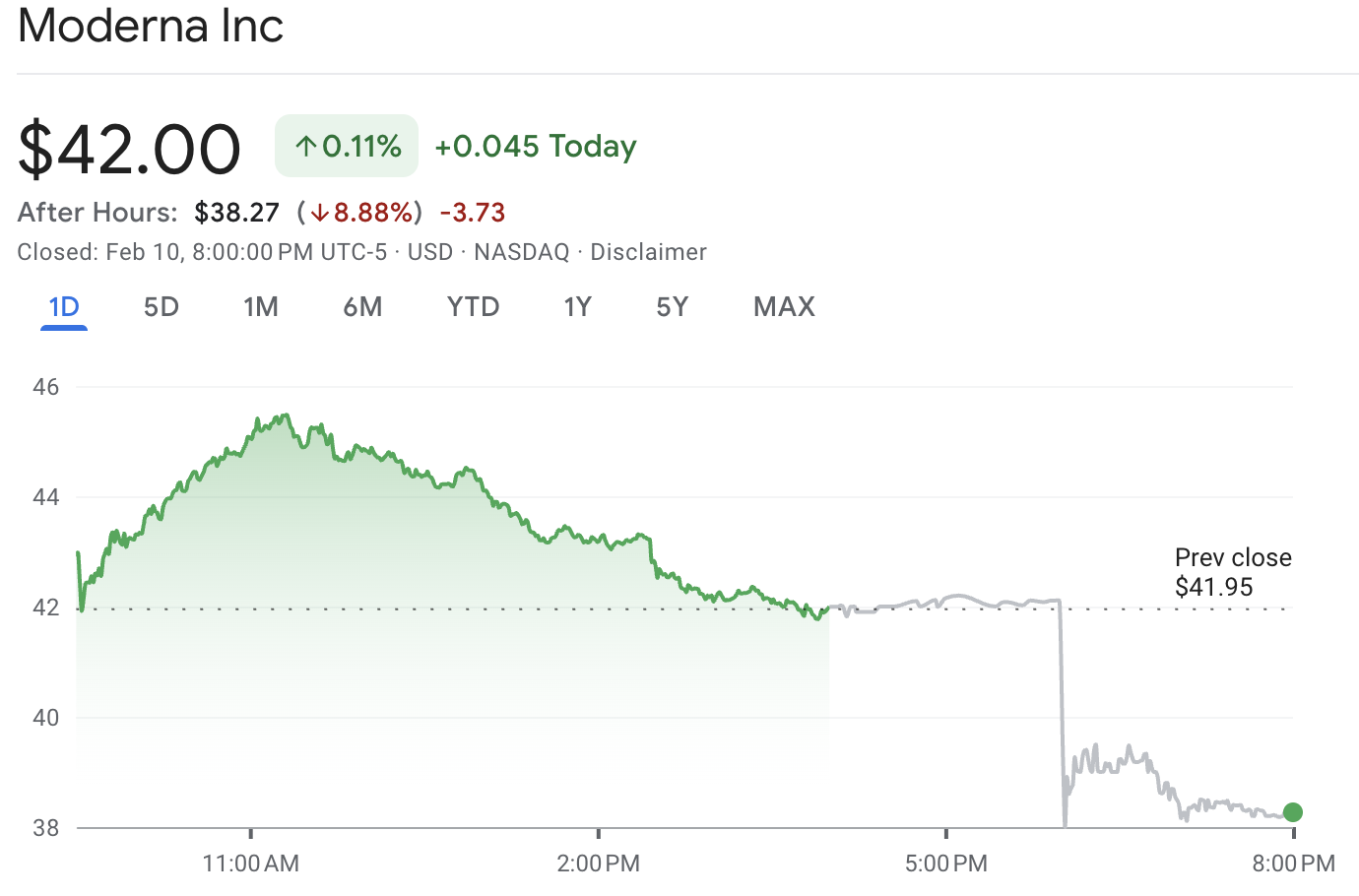
| Penutupan sesi reguler | ~$42.00 |
| Harga after-hours (contoh) | ~$38.27 (-8.88%) |
| Rentang hari | ~$41.68 hingga ~$45.50 |
| Rentang 52-minggu | ~$22.28 hingga ~$55.20 |
Saham MRNA ditutup sekitar $42.00 sebelum turun menjadi sekitar $38.27 dalam perdagangan after-hours, mencerminkan penurunan sekitar 8.9% pada saat laporan.

Moderna mengumumkan bahwa mereka menerima surat dari Pusat Evaluasi dan Penelitian Biologis FDA (CBER), yang menyatakan bahwa pihaknya tidak akan memulai tinjauan atas Biologics License Application (BLA) mRNA-1010 dan sebagai gantinya akan mengeluarkan surat Refusal to File (RTF).
Perusahaan menyoroti bahwa mereka telah memanfaatkan Priority Review Voucher untuk membantu memastikan tinjauan yang tepat waktu. Penolakan ini sangat mengecewakan bagi Moderna dari perspektif pasar, karena menunjukkan bahwa masalahnya bukan sekadar soal "dalam antrean."
Selain itu, Moderna mengindikasikan bahwa penolakan ini bertentangan dengan umpan balik yang diterimanya selama konsultasi pra-Fase 3 dan pra-pengajuan. Akibatnya, perusahaan telah meminta pertemuan Tipe A untuk memperjelas langkah selanjutnya.
RTF adalah alat formal yang digunakan FDA untuk menghindari menghabiskan waktu meninjau aplikasi yang dianggap tidak lengkap atau tidak cocok untuk tinjauan yang berarti pada tahap pengajuan.
Prosedur internal FDA mendefinisikan RTF sebagai metode untuk mencegah peninjauan yang tidak perlu terhadap aplikasi yang tidak lengkap. Hal ini menyoroti bahwa tindakan RTF memungkinkan pemohon untuk menangani "kekurangan kritis" sebelum mengajukan aplikasi lengkap, yang kemudian dapat menjalani tinjauan substantif.
Dua hal praktis penting bagi para trader:
RTF bukanlah persetujuan penuh maupun penolakan setelah tinjauan lengkap.
Jalan ke depan bergantung pada perubahan yang diminta FDA dan kemampuan perusahaan untuk merespons dengan cepat.

Isu sentral, sebagaimana dijelaskan dalam berbagai laporan, adalah bahwa FDA tidak menilai desain studi Moderna sebagai "memadai dan terkontrol dengan baik" karena lengan pembanding tidak mencerminkan pandangan FDA tentang standar perawatan terbaik yang tersedia, terutama untuk orang dewasa yang lebih tua.
Menurut pelaporan, Moderna membandingkan mRNA-1010 dengan vaksin flu ber-dosis standar yang berlisensi (sering dikutip sebagai Fluarix milik GSK dalam liputan).
Pada saat yang sama, FDA memberi sinyal bahwa mereka mengharapkan pembanding yang lebih sesuai dengan bagaimana populasi berisiko tinggi, khususnya yang berusia 65 tahun ke atas, umumnya divaksinasi di Amerika Serikat (seringkali dengan opsi yang ditingkatkan atau dosis tinggi).
Moderna menentang langkah ini. Dalam pernyataannya, perusahaan mengatakan RTF tersebut tidak menyebut isu keamanan atau kemanjuran dan menggambarkan keputusan itu tidak konsisten dengan umpan balik FDA sebelumnya.
FDA mengutip komparator dosis standar sebagai satu-satunya alasan menolak untuk memulai peninjauan.
Moderna menyatakan FDA tidak mengidentifikasi kekhawatiran khusus terkait keselamatan atau kemanjuran.
Moderna meminta pertemuan Tipe A dengan pimpinan FDA untuk memperjelas jalur ke depan.
Moderna menyatakan bahwa mereka tidak mengharapkan keputusan ini memengaruhi panduan keuangan 2026 mereka.
Pada uji vaksin, komparator adalah produk "dasar" yang digunakan untuk menilai kinerja produk baru. Jika regulator menilai komparator tidak mewakili standar dunia nyata yang tepat, regulator dapat berargumen bahwa bukti tersebut tidak menjawab pertanyaan yang perlu dijawabnya.
Itulah sebabnya pasar bereaksi kuat meskipun perusahaan mengatakan tidak ada kekhawatiran keselamatan baru. Perselisihan menggeser perdebatan dari "Apakah ini bekerja?" menjadi "Apakah bukti memenuhi standar FDA untuk populasi ini saat ini?"
Ini juga menjelaskan mengapa para pedagang sering memperlakukan berita RTF sebagai "peristiwa yang memengaruhi jadwal." Vaksin masih bisa mencapai pasar, tetapi waktunya menjadi kurang dapat diprediksi.
Moderna mengumumkan bahwa mRNA-1010 saat ini sedang ditinjau di UE, Kanada, dan Australia. Perusahaan memperkirakan bahwa persetujuan paling awal di wilayah-wilayah ini akan terjadi pada akhir 2026 atau awal 2027, berdasarkan evaluasi saat ini.
Di Amerika Serikat, langkah selanjutnya akan bergantung pada hasil pertemuan Tipe A. Hal ini akan menentukan apakah Moderna perlu mengirim ulang Biologics License Application (BLA) dengan data tambahan, pendekatan yang berbeda, atau pembingkaian ulang yang memenuhi ekspektasi FDA untuk komparator.
MRNA telah berusaha meyakinkan investor bahwa masa depannya pasca-COVID dibangun pada portofolio, bukan pada satu produk tunggal. Flu menjadi pusat narasi itu karena pasar pernapasan musiman besar, berulang, dan terbukti secara komersial.
Penolakan FDA ini memaksa penyesuaian pada tiga front.
Bahkan jika masalah tersebut dapat diselesaikan, RTF berarti Moderna tidak memiliki tinjauan FDA aktif yang sedang berlangsung hari ini. Itu saja mengurangi visibilitas jangka pendek dan memperbesar kesenjangan antara "data" dan "pendapatan."
Moderna telah menarik pengajuan ke FDA untuk vaksin kombinasi flu dan COVID mRNA-1083 setelah FDA meminta lebih banyak data tentang kemanjuran flu sebelum melanjutkan tinjauan. Sejarah itu penting karena pasar sudah pernah melihat jadwal respirasi Moderna bergeser.
Jika FDA kini menekankan komparator "standar perawatan terbaik yang tersedia" untuk orang dewasa yang lebih tua, itu bukan masalah pada satu program saja. Hal itu dapat membentuk bagaimana perusahaan merancang uji influenza di masa depan dan seberapa cepat mereka dapat melakukan iterasi.
Tanggal laporan pendapatan MRNA berikutnya dijadwalkan pada 13 Februari 2026, dan harga opsi mengantisipasi pergerakan implisit mingguan sekitar 11.63% menjelang jendela acara tersebut.
Pergerakan implisit di atas 10% biasanya memberi tahu bahwa investor mengharapkan ketidakpastian signifikan seputar berita, panduan, atau keduanya.
Setelah peristiwa penolakan pengajuan oleh FDA, pasar sering melakukan dua hal:
Menuntut bahasa yang lebih jelas mengenai langkah selanjutnya dan jadwal.
Menyesuaikan harga volatilitas implisit jika pasar mengharapkan komunikasi lanjutan, seperti hasil pertemuan FDA, terjadi di dekat jendela waktu yang sama.
| Indikator | Nilai | Sinyal |
|---|---|---|
| RSI (14) | 48.155 | Netral |
| MACD (12,26) | 0.29 | Beli |
| ATR (14) | 0.9374 | Volatilitas tinggi |
| ADX (14) | 40.829 | Jual |
Posisi teknikal harian MRNA secara umum netral, dengan sinyal yang bercampur di berbagai indikator dan rata-rata bergerak pada saat pergerakan di luar jam perdagangan.
| Jenis level | Tingkat harga | Bagaimana pelaku pasar sering menggunakannya setelah muncul headline |
|---|---|---|
| Klasik S1 | $41.74 | Area pertama di mana pembeli pada penurunan mungkin akan menguji jika pasar kembali stabil. |
| Klasik S2 | $41.31 | Penembusan ke bawah meningkatkan kemungkinan pengujian ulang level support yang lebih dalam. |
| Klasik S3 | $40.51 | Sebuah "garis" penting karena berada dekat dengan area kongesti rata-rata bergerak jangka panjang. |
| Pivot Klasik | $42.54 | Menguasai kembali pivot sering menandakan pasar mulai meredam kepanikan. |
| Klasik R1 | $42.97 | Titik pemeriksaan kenaikan pertama jika saham rebound memasuki periode laporan laba. |
| Klasik R2 | $43.77 | Zona rebound yang lebih kuat yang sering membutuhkan klarifikasi fundamental. |
Jika saham bertahan di atas area rendah-$40 selama jam perdagangan normal, hal ini menunjukkan pembeli masih mempertahankan tren.
Jika kelemahan dari perdagangan di luar jam berlangsung hingga sesi berikutnya dan harga tetap di bawah rata-rata bergerak kunci, sentimen pasar bisa tetap rapuh hingga muncul informasi baru.
Setelah jam perdagangan, saham MRNA turun menyusul pengumuman Moderna bahwa FDA mengeluarkan surat penolakan pengajuan (refusal-to-file) untuk BLA vaksin influenza mRNA-1010, yang menunjukkan bahwa FDA tidak akan memulai proses peninjauan.
Tidak. Pernyataan Moderna menunjukkan surat refusal-to-file tersebut tidak mengidentifikasi kekhawatiran keselamatan spesifik tentang mRNA-1010.
Karena vaksin pembanding adalah tolok ukur untuk menilai kinerja, dan FDA mengatakan vaksin pembanding yang digunakan tidak mencerminkan "standar perawatan terbaik yang tersedia," terutama untuk orang dewasa yang lebih tua.
Moderna mengatakan tidak mengharapkan adanya dampak terhadap panduan keuangan 2026 dari keputusan refusal-to-file tersebut. Investor tetap menjual saham karena waktu peluncuran program flu di AS penting untuk visibilitas pendapatan jangka panjang.
Ya. Moderna mengumumkan bahwa vaksin tersebut telah diterima untuk ditinjau di Uni Eropa, Kanada, dan Australia, dengan potensi persetujuan diperkirakan mulai akhir 2026 atau awal 2027.
Kesimpulannya, saham MRNA turun setelah jam perdagangan karena FDA mengeluarkan surat refusal-to-file untuk aplikasi vaksin flu mRNA Moderna, yang menimbulkan ketidakpastian jangka pendek terkait jadwal di AS.
Poin utamanya adalah bahwa pergerakan ini berkaitan dengan proses regulasi dan standar desain uji coba, bukan masalah keselamatan baru yang diungkapkan.
Faktor pembalikan berikutnya bukanlah perdebatan tentang imunologi influenza. Faktor pembalikan berikutnya adalah apakah Moderna dapat memperoleh jalur yang jelas ke depan melalui pertemuan Tipe A dengan FDA dan apakah jalur itu memerlukan pekerjaan klinis baru. Sampai kejelasan itu muncul, saham MRNA kemungkinan akan diperdagangkan sebagai saham yang sensitif terhadap headline dan bervolatilitas tinggi menjelang jendela laporan laba berikutnya.
Penafian: Materi ini hanya untuk keperluan informasi umum dan tidak dimaksudkan sebagai (dan tidak boleh dianggap sebagai) nasihat keuangan, investasi, atau nasihat lain yang dapat dijadikan dasar pertimbangan. Tidak ada opini yang disampaikan dalam materi ini yang merupakan rekomendasi oleh EBC atau penulis bahwa investasi, sekuritas, transaksi, atau strategi investasi tertentu cocok untuk orang tertentu.