تجارة
حول إي بي سي
اريخ النشر: 2026-02-11
انخفض سهم MRNA في التعاملات بعد الإغلاق لأن إدارة الغذاء والدواء (FDA) فرضت إيقافًا قاطعًا على برنامج كان المستثمرون يعتبرونه واحدًا من أكثر "جسور المنتج" الواقعية لموديرنا بعد امتيازها في مجال كوفيد.
أصدر مركز تقييم الأدوية البيولوجية والبحوث التابع لإدارة الغذاء والدواء (CBER) خطاب رفض قبول الطلب (Refusal-to-File, RTF) لطلب ترخيص الأدوية البيولوجية (BLA) الخاص بموديرنا للقاح الإنفلونزا الموسمي التجريبي mRNA-1010. كما أفاد بأنه لن يبدأ بمراجعة.

مع ذلك، تقول موديرنا إن الخطاب لم يثر مخاوف تتعلق بالسلامة أو الفعالية بشأن اللقاح نفسه، وأن القضية مرتبطة بذراع المقارنة المستخدم في دراسة الفعالية المرحلة 3.
بالنسبة للمتداولين، هذا يكفي لتحريك السهم بسرعة. عندما يصبح الجدول الزمني لمنتج رئيسي أقل وضوحًا، تميل الأسواق إلى إعادة تسعير المخاطر بسرعة، خاصة في التداول الممتد عندما تكون السيولة أضيق.
| البند | المستوى / التفاصيل |
|---|---|
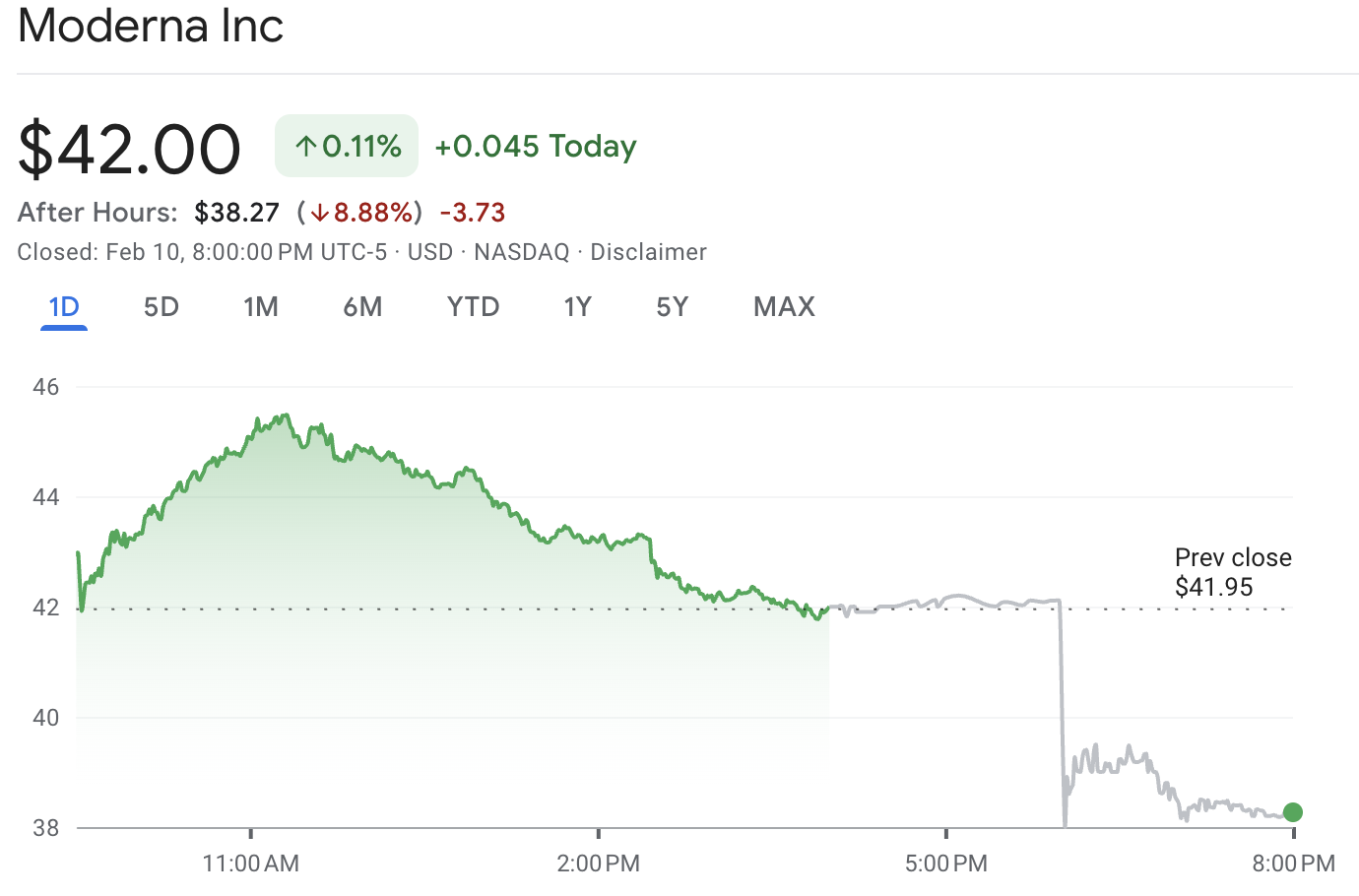
| إغلاق الجلسة العادية | ~$42.00 |
| سعر ما بعد الإغلاق (مثال) | ~$38.27 (-8.88%) |
| نطاق اليوم | ~$41.68 إلى ~$45.50 |
| نطاق 52 أسبوعًا | ~$22.28 إلى ~$55.20 |
أغلق سهم MRNA عند نحو $42.00 قبل أن ينخفض إلى حوالي $38.27 في تداولات ما بعد الإغلاق، ما يمثل تراجعًا بنحو 8.9% وقت التقرير.

أعلنت موديرنا أنها تلقت خطابًا من مركز تقييم الأدوية البيولوجية والبحوث التابع لإدارة الغذاء والدواء (CBER)، يفيد بأنها لن تبدأ مراجعة طلب ترخيص الأدوية البيولوجية (BLA) للـmRNA-1010، وبدلاً من ذلك ستصدر خطاب رفض قبول الطلب (Refusal to File, RTF).
أبرزت الشركة أنها استخدمت قسيمة مراجعة أولوية (Priority Review Voucher) للمساعدة في ضمان مراجعة في الوقت المناسب. هذا الرفض مخيب بشكل خاص لموديرنا من منظور السوق، إذ يوحي بأن القضية ليست مجرد كونها "في قائمة الانتظار".
وأضافت موديرنا أن هذا الرفض يتناقض مع الملاحظات التي تلقتها خلال المشاورات قبل المرحلة 3 وقبل تقديم الطلب. وبناءً عليه، طلبت الشركة عقد اجتماع من النوع A لتوضيح المسار المضي قدمًا.
الـRTF أداة رسمية تستخدمها إدارة الغذاء والدواء لتجنب قضاء الوقت في مراجعة طلبات تعتبرها غير مكتملة أو غير مناسبة لمراجعة موضوعية في مرحلة التقديم.
تعرف إجراءات الإدارة الداخلية الـRTF بأنها وسيلة لمنع المراجعة غير الضرورية للطلبات غير المكتملة. وتشير إلى أن إجراء الـRTF يسمح للمتقدمين بمعالجة "نواقص حرجة" قبل تقديم طلب كامل يمكن حينها الخضوع لمراجعة موضوعية.
نقطتان عمليتان تهمان المتداولين:
الـRTF ليس معادلاً للموافقة الكاملة أو الرفض بعد مراجعة كاملة.
المسار المستقبلي يعتمد على التغييرات التي تطلبها إدارة الغذاء والدواء (FDA) وقدرة الشركة على الاستجابة بسرعة.

المسألة الأساسية، كما وُصفت في تقارير متعددة، هي أن إدارة الغذاء والدواء (FDA) لم تعتبر تصميم دراسة موديرنا "كافيًا ومسيطرًا عليه جيدًا" لأن ذراع المقارنة لم يعكس وجهة نظر الـFDA حول أفضل مستوى رعاية متاح، لا سيما لكبار السن.
وفقًا للتقارير، قارنت موديرنا الـmRNA-1010 بلقاح إنفلونزا مرخّص بجرعة قياسية (يُشار إليه غالبًا على أنه Fluarix من GSK في التغطية).
وفي الوقت نفسه، أشارت إدارة الغذاء والدواء (FDA) إلى أنها كانت تتوقع مرجع مقارنة يطابق بشكل أفضل كيفية تطعيم الفئات عالية الخطورة، وخاصة من هم في سن 65 وما فوق، في الولايات المتحدة (غالبًا باستخدام خيارات معززة أو بجرعات عالية).
تعارض موديرنا هذا الإجراء. وفي بيانها قالت الشركة إن الـRTF لم يذكر مشكلات متعلقة بالسلامة أو الفعالية ووصف القرار بأنه يتعارض مع ملاحظات سابقة من الـFDA.
ذكرت الـ FDA أن المقارن بجرعة قياسية كان السبب الوحيد في رفض بدء المراجعة.
قالت Moderna إن الـ FDA لم تحدد مخاوف محددة تتعلق بالسلامة أو الفعالية.
طلبت Moderna عقد اجتماع من النوع A مع قيادة الـ FDA لتوضيح مسار المضي قدمًا.
أفادت Moderna أنها لا تتوقع أن يؤثر هذا القرار على توقعاتها المالية لعام 2026.
في تجارب اللقاحات، يُعد المقارن المنتج «الأساسي» المستخدم للحكم على أداء المنتج الجديد. إذا اعتقد المنظم أن المقارن لا يمثل المعيار الواقعي المناسب، فقد يجادل بأن الأدلة لا تجيب عن السؤال الذي يحتاج إلى إجابة.
لهذا تتفاعل الأسواق بقوة حتى عندما تقول الشركة إنه لا توجد مخاوف سلامة جديدة. تتحول المناقشة من «هل هو فعال؟» إلى «هل تلبي الأدلة معيار الـ FDA لهذه الفئة السكانية في الوقت الراهن؟»
هذا يفسر أيضًا لماذا يعتبر المتداولون غالبًا عناوين RTF كـ"أحداث في الجدول الزمني." قد يصل اللقاح إلى السوق في نهاية المطاف، لكن توقيت ذلك يصبح أقل قابلية للتنبؤ.
أعلنت Moderna أن mRNA-1010 قيد المراجعة حاليًا في الاتحاد الأوروبي وكندا وأستراليا. تتوقع الشركة أن تحدث أول الموافقات في هذه المناطق في أواخر 2026 أو أوائل 2027، استنادًا إلى التقييمات الحالية.
في الولايات المتحدة، ستعتمد الخطوات التالية على نتيجة اجتماع من النوع A. سيحدد ذلك ما إذا كانت Moderna بحاجة إلى إعادة تقديم طلب ترخيص المستحضرات البيولوجية (BLA) مع بيانات إضافية أو نهج مختلف أو صياغة معدلة تلبي توقعات الـ FDA بشأن المقارنات.
تحاول MRNA إقناع المستثمرين بأن مستقبلها بعد كوفيد مبني على محفظة منتجات، وليس على منتج واحد. تلعب الإنفلونزا دورًا محوريًا في هذه الرواية لأن أسواق الأمراض التنفسية الموسمية كبيرة ومتكررة ومثبتة تجاريًا.
يفرض هذا الرفض من الـ FDA إعادة ضبط على ثلاثة أصعدة.
حتى لو كان يمكن حل المشكلة، فإن RTF يعني أن Moderna ليس لديها مراجعة نشطة لدى الـ FDA تجري اليوم. هذا وحده يقلل الرؤية على المدى القريب ويزيد الفجوة بين 'البيانات' و'الإيرادات'.
سحبت Moderna ملفها لدى الـ FDA للقاح المدمج mRNA-1083 للإنفلونزا وكوفيد بعد أن طلبت الـ FDA مزيدًا من البيانات حول فعالية الإنفلونزا قبل المضي في المراجعة. لهذه الخلفية أهمية لأن السوق سبق وأن شاهد انزلاق الجدول الزمني لمنتجات Moderna التنفسية مرة واحدة.
إذا كانت الـ FDA تؤكد الآن على المقارنات القائمة على «أفضل معيار رعاية متاح» لكبار السن، فهذه ليست مسألة تخص برنامجًا واحدًا فقط. يمكن أن تشكل كيفية تصميم الشركات لتجارب الإنفلونزا المستقبلية ومدى سرعتها في التكرار.
موعد إعلان نتائج MRNA المجدول التالي هو 13 فبراير 2026، وتسعر الخيارات تحركًا ضمنيًا أسبوعيًا بنحو 11.63% خلال نافذة ذلك الحدث.
عادةً ما يدل تحرك ضمني فوق 10% على أن المستثمرين يتوقعون عدم يقين جوهري حول العناوين أو التوجيهات أو كليهما.
بعد حدث رفض تقديم ملف لدى الـ FDA، غالبًا ما يفعل السوق أمرين:
يطالب بلغة أوضح لمسار المضي قدمًا والجداول الزمنية.
يُعيد تسعير التقلب الضمني إذا كان يتوقع أن يحدث تواصل متابعة، مثل نتيجة اجتماع مع الـ FDA، في نافذة زمنية قريبة من نفس الفترة.
| المؤشر | القيمة | الإشارة |
|---|---|---|
| RSI (14) | 48.155 | محايد |
| MACD (12,26) | 0.29 | شراء |
| ATR (14) | 0.9374 | تقلب مرتفع |
| ADX (14) | 40.829 | بيع |
كان الوضع الفني اليومي لسهم MRNA محايدًا إلى حدٍ بعيد، مع إشارات متباينة عبر المؤشرات والمتوسطات المتحركة في وقت حركة ما بعد ساعات التداول.
| نوع المستوى | مستوى السعر | كيف يستخدمه المتداولون غالبًا بعد ظهور خبر |
|---|---|---|
| S1 الكلاسيكي | $41.74 | أول منطقة قد يختبرها مشترُو الانخفاضات إذا استقر التداول. |
| S2 الكلاسيكي | $41.31 | كسر أدناه يزيد من احتمالات إعادة اختبار مستويات دعم أعمق. |
| S3 الكلاسيكي | $40.51 | خط مهم لأنه يقع قرب تكتل المتوسطات المتحركة الطويلة الأجل. |
| محور كلاسيكي | $42.54 | غالبًا ما تشير استعادة المحور إلى أن السوق يتلاشى من الذعر. |
| R1 الكلاسيكي | $42.97 | أول نقطة تفتيش صعودية إذا ارتد السهم مع اقتراب موسم النتائج. |
| R2 الكلاسيكي | $43.77 | منطقة ارتداد أقوى غالبًا ما تتطلب توضيحًا أساسيًا. |
إذا ظل السهم فوق منطقة أوائل الأربعين خلال ساعات التداول العادية، فهذا يوحي بأن المشترين لا يزالون يدافعون عن الاتجاه.
إذا استمرت الضغوط الهابطة من ما بعد ساعات التداول إلى الجلسة التالية وبقي السعر أسفل المتوسطات المتحركة الرئيسية، فقد تظل معنويات السوق هشة حتى ظهور معلومات جديدة.
بعد الإغلاق، هبط سهم MRNA بعد إعلان موديرنا أن إدارة الغذاء والدواء (FDA) أصدرت رسالة رفض لتقديم الطلب (refusal-to-file) لطلب ترخيص منتج BLA الخاص بلقاح mRNA-1010 للإنفلونزا، ما يشير إلى أن FDA لن تبدأ مراجعة.
لا. يشير بيان موديرنا إلى أن رسالة الرفض لتقديم الطلب لم تحدد مخاوف سلامة محددة بشأن mRNA-1010.
لأن لقاح المقارنة هو المعيار المرجعي لتقييم الأداء، وقالت FDA إن لقاح المقارنة المستخدم لم يعكس «أفضل معيار متاح للرعاية»، لا سيما بالنسبة لكبار السن.
قالت موديرنا إنها لا تتوقع أي تأثير على توجيهاتها المالية لعام 2026 نتيجة قرار الرفض لتقديم الطلب. مع ذلك باع المستثمرون السهم لأن توقيت برنامج الإنفلونزا في الولايات المتحدة مهم للرؤية الإيرادية على المدى الأطول.
نعم. أعلنت موديرنا أن اللقاح قُبل للمراجعة في الاتحاد الأوروبي (EU) وكندا وأستراليا، مع توقع أن تبدأ الموافقات المحتملة في أواخر 2026 أو أوائل 2027.
خلاصة القول، انخفض سهم MRNA بعد ساعات التداول لأن FDA أصدرت رسالة رفض لتقديم الطلب لطلب موديرنا للقاح الإنفلونزا mRNA، ما يثير عدم يقين قصير المدى حول الجدول الزمني في الولايات المتحدة.
النقطة الأساسية هي أن هذه الحركة تتعلق بإجراءات تنظيمية ومعايير تصميم التجارب، وليست بمشكلة سلامة جديدة تم الكشف عنها.
عامل التحول التالي ليس نقاشًا في مناعة الإنفلونزا. العامل التالي هو ما إذا كانت موديرنا تستطيع تأمين مسار واضح للمضي قدمًا من خلال اجتماع من نوع Type A مع FDA وما إذا كان ذلك المسار يتطلب أعمالًا سريرية جديدة. حتى وصول ذلك الوضوح، من المرجح أن يتداول سهم MRNA كسهم حساس للعناوين وعالي التقلب خلال نافذة النتائج التالية.
إخلاء المسؤولية: هذه المادة معدة لأغراض المعلومات العامة فقط وليست مقصودة (ولا ينبغي اعتبارها) نصيحة مالية أو استثمارية أو غيرها يُعتمد عليها. لا تشكل أي رأي وارد في المادة توصية من EBC أو من المؤلف بأن أي استثمار أو ورقة مالية أو صفقة أو استراتيجية استثمار مناسبة لأي شخص بعينه.